Erste Kontakte mit einem Muskelrelaxans (MR) hatte die "zivilisierte Welt" im Jahre 1492. Es wurde damals natürlich nicht als Medikament verwendet sondern diente den Indianern als Pfeilgift.
In diesem Beitrag werden die verschiedenen Gruppen der Relaxanzien sowie deren Eigenschaften vorgestellt.
Inhalt
- Einleitung, Geschichte
- Neuromuskuläre Reizübertragung
- Gruppen von Muskelrelaxanzien
- Nichtdepolarisierende MR
- Depolarisierende MR
- Kennzahlen
- neuromuskuläres Monitoring
- Literatur
Einleitung / Geschichte
Erste Kontakte mit einem Muskelrelaxans (MR) hatte die "zivilisierte Welt" im Jahre 1492. Es wurde damals natürlich nicht als Medikament verwendet sondern diente den Indianern als Pfeilgift.
Als Columbus auf dem Weg nach Indien Amerika entdeckte und kolonisierte kam es mit den Ureinwohnernzu Streitigkeiten. Die "unzivilisierten Wilden" verteidigten sich mit Pfeilen gegen die Kolonialherren. Es wird berichtet, dass selbst harmlose Verletzungen durch Indianerpfeile bei den Matrosen Columbus innerhalb weniger Minuten zum Tod führten.
Das Gift, welches die Einwohner von Amazonas und Orinoko normalerweise für die Jagd einsetzten stammte von den Pflanzen Chondodendron tomentosum (»Curare) und Strychnos toxifera. 1812 injizierte B.C. Brodi einer tracheotomierten und beatmeten Katze eine sonst tödliche Dosis Tubocurarin. Nach ca. 40 Minuten wachte die Katze auf und lief davon.
Zwischen 1850 und 1857 forschte Claude Bernard über Curare. Er stellte dabei unter anderem fest, ...
- ...dass Curare nur bei direkter Verabreichung in die Blutbahn wirkt.
- ...dass der Tod durch Lähmung der Muskulatur eintritt, wobei die Herzmuskulatur nicht gelähmt wird.
- ...dass Curare auf die Übertragung der Impulse zwischen motorischen Nerven und Muskulatur wirkt. Sensorische Nerven sind nicht betroffen.
- ...dass periphere Muskeln am stärksten betroffen sind, dann die thorakale Muskulatur und das Zwerchfell.
Am 23. Januar 1942 injizierte Griffith zum ersten mal einem jungen Mann Intocostrin (Curare-Präparat) bei einer Appendektomie. Nach seinen Berichten erschlaffte die Bauchmuskulatur, eine Ateminsuffizienz trat aber nicht auf (Dosis). Dieses Datum gilt als Meilenstein in der Geschichte der modernen Anästhesie.
Neuromuskuläre Reizübertragung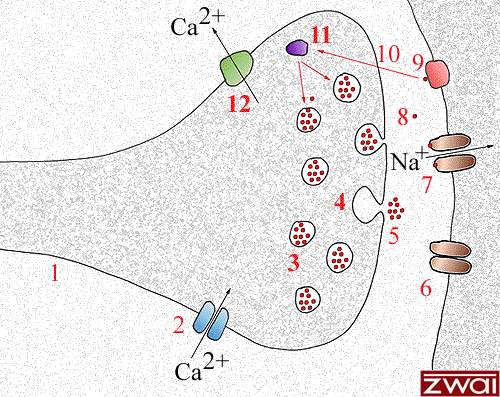
Abb. 1: motorische Endplatte - mit freundlicher Genehmigung von Ulrich Helmich
1. Motorischer Nervenimpuls breitet sich über efferente Nervenfasern vom ZNS nach peripher aus.
2. Das Aktionspotential kommt am Endkolben des 2. Motoneurons an (myoneuronale Synapse). Dort werden durch die Spannungsänderung Kalziumionenkanäle geöffnet und Kalzium diffundiert in die Nervenzelle.
3. Dadurch bewegen sich acethylcholinhaltige Vesikel zur präsynaptischen Membran, verschmelzen mit ihr.
4. / 5. Das ACh wird in den subsynaptischen Spalt entleert (Exozytose).
(6. Ein geschlossener Natriumkanal)
7. / 8. Das freigesetzte ACh überwindet den Synapsenspalt und dockt an den ACh-Rezeptoren der postsynaptischen Membran an. Die ACh-Rezeptoren öffnen ihre Ionenkanäle und es kommt zu einem Natriumeinstrom in und Kaliumausstrom aus der postsynaptischen Membran. Durch diese Spannungsänderung werden an der postsynaptische Membran Kalziumkanäle geöffnet und Kalzium diffundiert in die Muskelzelle. (à Muskelkontraktion).
9. Das ACh löst sich wieder vom Rezeptor und wird von der Acetylcholinesterase in Acetat und Cholin gespalten.
10. Die Spaltprodukte werden durch die präsynaptische Membran wieder in die Nervenzelle aufgenommen...
11. ... und stehen zur Neusynthese von ACh zur Verfügung.
12. Die bei Schritt 2 eingedrungenen Calciumionen werden wieder aus der Zelle herausgepumpt (ATP-Verbrauch)
Gruppen von Muskelrelaxanzien
| Periphere MR | Zentrale MR |
|
|
Je nach Wirkdauer unterscheidet man:
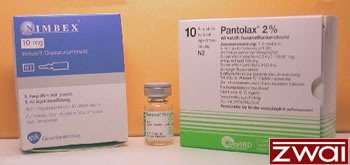
- Kurzwirksame NDMR: Mivacurium, Rapacuronium
- Mittellangwirksame NDMR: Atracurium, cis-Atracurium (Nimbex®), Rocuronium (Esmeron®), Vecuronium (Norcuron®)
- Langwirksame NDMR: Tubocurarin, Alcuronium (Alloferin®), Pancuronium, Doxacurium
Abb. 2: Muskelrelaxanzien (v.l.n.r.: Nimbex®, Esmeron®, Pantolax®)
Indikation für den Einsatz von peripher wirkenden Muskelrelaxanzien:
- Erleichterung der Intubation
- Verhinderung von Muskelbewegungen während einer OP (Darm-OP)
Nichtdepolarisierende Muskelrelaxanzien
Wirkung
Sie binden an die Acetylcholinrezeptoren der postsynaptischen Membran ohne dort eine Depolarisation auszulösen.
Sie wirken pharmakologisch also als kompetitiver Antagonist (kompetitive Verdrängung). Ist die Konzentration an nichtdepolarisierendem Muskelrelaxans ausreichend hoch, sind also alle Acetylcholinrezeptoren besetzt, kann das Acetylcholin keine Impulse mehr übertragen.
Wirkungseintritt
Zuerst werden kleine Muskeln relaxiert (an Auge, Ohr, Finger).
Es folgen Muskeln der Extremitäten, an Hals und Stamm; zuletzt die Intercostalmuskulatur und das Diaphragma.
Die Rückkehr der Muskelkraft erfolgt in umgekehrter Reihenfolge. (kann der Patient den Kopf für länger als 5s anheben, kann davon ausgegangen werden, dass die Atemmuskulatur auch erholt ist und der Patient spontan atmen kann)
Eine Beschleunigung des Wirkeintritts kann durch das Priming erreicht werden. Hier wird ca. 1/10 der Intubationsdosis zu Beginn der Einleitung gegeben um einen Teil der Rezeptoren zu besetzen. Die eigentliche Relaxierung geht dann schneller von statten.
Wirkbeendigung
Da die Relaxanzien nicht durch die Acetylcholinesterase gespalten werden, dauert die Blockierung des Rezeptors für eine gewisse Zeit an. Die Dauer der Blockierung ist eine stoffspezifische Eigenschaft des jeweiligen Muskelrelaxans.
Die Verminderung der Wirkung bzw. das Wirkende wird erreicht durch:
- Umverteilung im Körper, MR diffundieren vom Rezeptor ab und werden über Blut und Lymphe abtransportiert.
- Ausscheidung, vor allem über die Niere (cave: Niereninsuffizienz!) und teilweise über die Galle
- Zu geringem Teil Abbau über die Leber. ( cave: Leberschäden, Zirrhose!)
- Enzymatischer Abbau durch die Pseudocholinesterase
- Ausnahmen: cis-Atracurium; wird gänzlich enzymunabhängig abgebaut. Es "zerfällt" in unwirksame Bestandteile. (ß Hoffmann-Elimination); Atracurium zerfällt zum Teil enzymunabhängig, zum Teil wird es durch die Pseudocholinesterase gespalten.
Nebenwirkungen
- auf das vegetative Nervensystem: Hyper-/Hypotonie, Sinustachykardie, Arrhythmie
- durch Histaminfreisetzung (hauptsächlich bei Tubocurarin): Hypotonie, Tachykardie, Bronchokonstriktion, Erythem(Gesicht/oberer Stamm), Freisetzung von Kalium, Katecholaminen und Heparin
Antagonisierung
Nichtdepolarisierende Muskelrelaxanzien können durch die Gabe von Cholinesterasehemmern (Neostigmin, Pyridostigmin) antagonisiert werden. Durch die Hemmung der Cholinesterase sammelt sich Acetylcholin im synaptischen Spalt an. Durch die zunehmende Konzentration verdrängt das Acetylcholin jetzt das Muskelrelaxans (kompetitive Verdrängung) vom Rezeptor.
CAVE: Cholinesterasehemmer (Parasympathomimetika) wirken auch am 1. Neuron (präganglionär) und es kommt so zu einer verstärkten Aktivität des Parasympathikus mit den möglichen Nebenwirkungen:
- Bradykardie
- Vermehrte Produktion von Speichel und Bronchialsekret
- Krampfzustände der glatten Muskulatur (Darm und Bronchialsystem)
Zur Verminderung dieser Nebenwirkungen kann Atropin (Parasympatholytikum) eingesetzt werden. Trotzdem ist bei Patienten mit Asthma bronchiale, Bradykardien und AV-Blockierungen bei der Antagonisierung Vorsicht geboten.
Depolarisierende Muskelrelaxanzien
Das einzige gebräuchliche depolarisierende Muskelrelaxans ist das Succinylcholin. Sein klinischer Einsatz wird heiß diskutiert wegen der teilweise lebensbedrohlichen Nebenwirkungen.
Die Indikation für die Verwendung von Succinyl zur Relaxierung besteht nur, wenn ein sehr schneller Wirkeintritt erforderlich ist. Also bei der Rapid Sequence Induction von nicht nüchternen Patienten, bei Schwangeren zur Sectio und bei OPs bis zu zwei Wochen post partum.
Ob die Kürze der OP (z.B. HNO: TE, AT) als Indikation für die Einleitung mit Succinyl ausreicht ist sicher diskussionswürdig.
Wirkung & Wirkbeendigung
Sie binden auch an die Acetylcholinrezeptoren der postsynaptischen Membran, bewirken dort sehr schnell eine Depolarisation (wie das Acetylcholin), werden aber nicht durch die im Synapsenspalt vorliegende spezifische Cholinesterase abgebaut.
So bewirken sie eine Dauerdepolarisation die eine weitere Erregbarkeit des Muskels verhindert (refraktär). Die depolarisierenden Muskelrelaxanzien werden, nach Abdiffusion aus dem Synapsenspalt in die Blutbahn, durch die Pseudocholinesterase im Serum rasch abgebaut, weshalb ihre Wirkdauer relativ kurz ist (ca. 5 min).
Nach Gabe einer Einzeldosis wird ein Phase-1-Block (wie oben beschrieben) erreicht, der nicht antagonisierbar ist. Wird während der Narkose mehrmals ein depolarisierendes Muskelrelaxans nachinjiziert oder als Dauerinfusion appliziert wird ein Phase-II-Block erreicht (Dualblock).
Je nach Quelle wird die Dosis für den Dualblock mit 300 bis 500mg Gesamtdosis angegeben. Beim Phase-II-Block besteht keine Depolarisation mehr obwohl keine kompetitive Wirkung nachweisbar ist. Die Nervenblockade bleibt aber erhalten. Dieses Relaxierungsstadium ist durch Cholinesterasehemmer in gewissem Maße antagonisierbar.
Nebenwirkungen
- Triggersubstanz für die maligne Hyperthermie.
- Prolongierte Wirkdauer der Relaxierung bei Pseudochlinerterase-Mangel
- Rhythmusstörungen/Herzstillstand durch Erhöhung der Kaliumkonzentration nach Succinylgabe. Besonders bei Patienten mit Hemiplegie, längerfristig immobilen Patienten, nach massivem Muskeltrauma, nach Verbrennungen (jeweils Kontraindikationen)
- Rhythmusstörungen/Herzstillstand durch die direkte Stimulation parasympathischer muskarinerger Ganglien
- Rhythmusstörungen bis hin zum Kammerflimmern (besonders bei Kindern) durch Wirkung der Abbauprodukte des Succinyl auf das vegetative Nervensystem. Succinylbedingte Bradikardien können in der Regel mit ¼ - ½ mg Atropin iv. behoben werden.
- Vorsicht bei katecholaminpflichtigen Patienten (Wechselwirkung mit Succinyl): vermehrt ventrikuläre Extrasystolen.
- Muskelfaszikulationen "Muskelkater" bis zum 1.postOP-Tag
- Kontraindiziert (?) bei Kindern, Neugeborenen und Säuglingen weil hier schon lebensbedrohliche Zustände beobachtet wurden. (Rabdomyolyse, Hyperkaliämie, Myoglobinämie, schwere Azidose) jeweils mit hoher Mortalität.
Muskelfaszikulationen, Muskelkater und Kaliumanstieg können durch die Vorgabe eines nichtdepolarisierenden Muskelrelaxans vermindert werden (Präcurarisierung)
Kennzahlen
Um die Relaxanzien bezüglich ihrer neuromuskuären Potenz und dem Verlauf der Blockade vergleichen zu können wurden die u.g. stoffspezifischen Kennzahlen eingeführt.
Anschlagszeit: Beschreibt die Zeit vom Ende der iv. Injektion bis zum Eintritt der maximalen Wirkung eines Relaxans.
ED95: Beschreibt die Dosis eine Muskelrelaxans, die zu einer 95%igen neuromuskulären Blockade führt. [mg/kgKG oder µg/kgKG]
Intubationsdosis: Dosis, mit der eine für die endotracheale Intubation ausreichende Relaxierung erreicht wird. Meist das 2-3 fache der ED95.
DUR25: (Klinische Wirkdauer) Die Zeit von der Injektion des Relaxans bis zum Abklingen der neuromuskulären Blockade auf 25% des Ausgangswerts. Während dieser Zeitspanne ist der Patient für die meisten Eingriffe ausreichend relaxiert. Diese Kennzahl wird verwendet um die Relaxanzien in drei Gruppen bezüglich ihrer Wirkdauer einzuteilen.
- kurz wirkende MR : DUR25 < 20 min
- mittellang wirkende MR : DUR25 20-50 min
- lang wirkende MR : DUR25 > 50 min
DUR95: (Gesamtwirkdauer) Zeit zwischen dem Ende der Injektion bis zum Nachlassen der Blockade auf 95% des Ausgangswerts. Sie beträgt im Allgemeinen das 2fache der DUR25. Nach dieser Zeit können die Patienten in der Regel extubiert werden.
RI: ("recovery index", Erholungszeit) Die Zeit zwischen 25- und 75%iger Erholung der neuromuskulären Blockade.
neuromuskuläres Monitoring
Ergänzung der Redaktion
"Muskelrelaxanzien weisen nicht nur bezüglich ihrer Anschlagzeit eine große interindividuelle Variabilität auf; auch ihre Wirkdauer unterliegt ausgeprägten individuellen Schwankungen.
So fand Katz nach Gabe von 0,1 mg/kg d-Tubocurarin bei 6 von 100 Patienten keine nachweisbare Wirkung, während 7 Patienten eine komplette neuromuskuläre Blockade entwickelten. Wenn auch die Mehrzahl der Patienten eine für diese Dosis zu erwartende Blockade von 40 bis 70% aufwies, so zeigt diese Untersuchung doch deutlich, dass für den individuellen Patienten das Ausmaß der zu erwartenden Blockade nicht einmal annähernd vorhergesagt werden kann. Ähnliches gilt für Atracurium und Vecuronium.
Für die neueren Substanzen wie Mivacurium, Cisatracurium und Rocuronium liegen keine diesbezüglichen Untersuchungen vor, jedoch kann man ähnliche Verhältnisse unterstellen. Die zur Umgehung der Problematik der individuell variierenden Anschlagzeit bewährte Praxis, zur Narkoseeinleitung die doppelte ED95 zu verabreichen, ist für die intraoperative Phase kein gangbarer Weg. Hinzu kommt, dass Interaktionen mit anderen Anästhetika, insbesondere Inhalationsanästhetika, aber auch beispielsweise Antibiotika, Diuretika und Antihistaminika die Wirkdauer von Muskelrelaxanzien verändern und somit eine den Erfordernissen des intraoperativen Verlaufs angepasste Steuerung der neuromuskulären Blockade zusätzlich erschweren.
Ein quantitatives neuromuskuläres Monitoring (TOF-Ratio) ist daher unerlässlich, um Restblockaden am Ende einer Operation zu erkennen und könnte darüber hinaus bereits bei der Einleitung der Anästhesie wertvolle Informationen liefern, etwa über den optimalen Intubationszeitpunkt.
Für den Einsatz in der anästhesiologischen Praxis stehen heute eine Reihe von technisch ausgereiften, relativ einfach zu bedienenden Relaxometern (meist Akzelerographen oder Elektromyographen) mit allen gängigen Stimulationsmustern (Einzelreizung, Train-of-Four-Stimulation (TOF) , Double-Burst-Stimulation (DBS), und Tetanus mit Bestimmung des sog. Post-Tetanic-Count (PTC)) zur Verfügung."
Anaesthesist 49 (2000) 13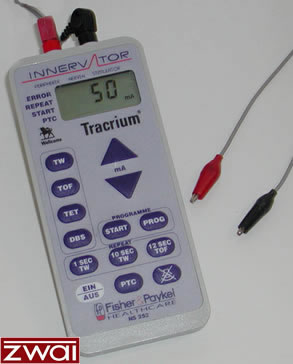
Abb. 3: Relaxometer "Innervator Fisher Paykel"
Literatur
- Dudziak R; Muskelrelaxanzien - Ein Kompendium. Steinkopff Verlag, Darmstadt, 2001
- Larsen , R. Anästhesie und Intensivmedizin für Schwestern und Pfleger - Springer Verlag Berlin, 5. Auflage, 1999
- Latasch, Ruck, Seiz Anästhesie, Intensivmedizin und Intensivpflege - Urban und Fischer Verlag München, 1999
- Striebel, H.W. Anästhesie und Intensivmedizin für Studium und Pflege - Schattauer Verlag Stuttgart, 4. Auflage, 2000
- Martin, E. Facharztlehrbuch Anästhesiologie - Blackwell Wissenschaft Verlag Berlin, 1997
- Brandl P, Muskelrelaxanzien -intensiv, 1999; 7: 204 - 211
- Rieke, Kurs der allgemeinen Pharmakologie, 01.05.2001
< http://www.medizin.fu-berlin.de/copharma/students/pdf/NarkoseAllg.pdf > - Anaesthesist 49 (2000) 13
Abbildungen
Abb. 1.: Ulrich Helmich, http://www.u-helmich.de, 12.09.2002 - mit freundlicher Genehmigung
Abb. 2.: Redaktion zwai.net / hhe
Abb. 3.: Redaktion zwai.net / hhe